Pertanyaan Tentang Elektrolisis. Berapa alumunium dapat diperoleh setiap jam jika digunakan arus 100 ampere. Seperti yang telah kita pelajari, s el elektrolisis adalah sel yang mengubah energi listrik menjadi energi kimia. Hukum ohm, tegangan peruraian, tegangan polarisasi, tegangan berlebih dan potensial standar. Memahami,menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural berdasarkan rasa ingintahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasankemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang.
 Tentukan reaksi elektrolisis yang terjadi pada larutan From brainly.co.id
Tentukan reaksi elektrolisis yang terjadi pada larutan From brainly.co.id
Reduksi ion alkali terjadi di anoda. Seperti yang telah kita pelajari, s el elektrolisis adalah sel yang mengubah energi listrik menjadi energi kimia. Pada elektrolisis larutan znso4 terjadi reduksi zn2+ menjadi zn. Di anode dihasilkan gas oksigen. Dibuat dari elektrolisis larutan garam kloridanya. Mereka adalah berilium (be), magnesium (mg), kalsium (ca), stronsium (sr), barium (ba), dan radium (ra).
Reduksi ion logam alkali terjadi dianode.
Berapa alumunium dapat diperoleh setiap jam jika digunakan arus 100 ampere. Pada elektrolisis cuso 4 dihasilkan 25,4 gram endapan cu pada katoda. Elektrokimia merupakan salah satu materi kimia yang cukup menarik untuk dibahas. Reduksi ion alkali terjadi di anoda. Pada elektrolisis anode dihubungkan dengan kutub positif sumber energi listrik, sedangkan katode dihubungkan dengan kutub negatif. Mereka adalah berilium (be), magnesium (mg), kalsium (ca), stronsium (sr), barium (ba), dan radium (ra).
 Source: brainly.co.id
Source: brainly.co.id
Oleh karena itu pada sel elektrolisis di anode akan terjadi reaksi oksidasi dan dikatode akan terjadi reaksi reduksi. Sekian dulu pembahasan mengenai elektrolisis, tinggalkan komentar jika ada yang dirasa kurang jelas, semoga bermanfaat. F = jumlah arus listrik dalam satuan faraday. Pada elektrolisis anode dihubungkan dengan kutub positif sumber energi listrik, sedangkan katode dihubungkan dengan kutub negatif. Tak lupa, telah tersedia pula latihan soal yang bisa coba kamu kerjakan.
 Source: studyassistant-id.com
Source: studyassistant-id.com
Ion logam alkali yang terbentuk berupa zat padat di anode. Seperti yang telah kita pelajari, s el elektrolisis adalah sel yang mengubah energi listrik menjadi energi kimia. F = jumlah arus listrik dalam satuan faraday. Logam alkali yang terbentuk berupa zat padat dianoda. Arus listrik digunakan untuk melangsungkan reaksi redoks tak spontan.
 Source: brainly.co.id
Source: brainly.co.id
Digunakan katoda karbon dan anoda dari besi. Jadi pernyataan yang benar adalah. Seperti yang telah kita pelajari, s el elektrolisis adalah sel yang mengubah energi listrik menjadi energi kimia. Untuk mempelajari materi tentang sel elektrolisis dan hukum faraday, kalian. F = jumlah arus listrik dalam satuan faraday.
 Source: brainly.co.id
Source: brainly.co.id
Pernyataan berikut ini yang benar tentang zat yang teroksidasi di anoda dan tereduksi di katoda pada proses elektrolisis larutan dan lelehan adalah. Untuk lebih meningkatkan pengetahuanmu mengenai materi elektrokimia, perhatikan 5 soal elektrokimia dan penyelesaiannya berikut ini! Dalam elektrolisis larutan cuso 4, diharapakan logam cu dapat mengendap sebanyak 2,54 g pada katode. Apakah kamu sedang mencari pembahasan mengenai materi elektrolisis? 10 contoh soal elektrolisis kelas 12 beserta jawabannya.
 Source: brainly.co.id
Source: brainly.co.id
Lewat pembahasan ini, kamu bisa belajar mengenai elektrolisis. Pernyataan yang tepat tentang pembuatan logam alkali secara elektrolisis adalah. Di katode dihasilkan gas hidrogen. Apakah kamu sedang mencari pembahasan mengenai materi elektrolisis? Soal no.1 (sbmptn 2017) elektrolisis 100 ml larutan cuso 4 0,1 m dalam bejana a dan 100 ml larutan agno 3 dalam bejana b dilakukan seri menggunakan arus tetap 1 a pada anoda dan katoda pt.
 Source: brainly.co.id
Source: brainly.co.id
Untuk lebih meningkatkan pengetahuanmu mengenai materi elektrokimia, perhatikan 5 soal elektrokimia dan penyelesaiannya berikut ini! Logam alkali mengalami reaksi reduksi. F = jumlah arus listrik dalam satuan faraday. Modul, rumus, & soal elektrokimia. Elektrokimia merupakan salah satu materi kimia yang cukup menarik untuk dibahas.
 Source: studyassistant-id.com
Source: studyassistant-id.com
Ar ag = 108 dan konstanta farady = 96500 c/mol). Modul, rumus, & soal elektrokimia. Di anode dihasilkan gas oksigen. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal. Soal ini diselesaikan dengan hukum faraday i, dengan rumusan:
 Source: brainly.co.id
Source: brainly.co.id
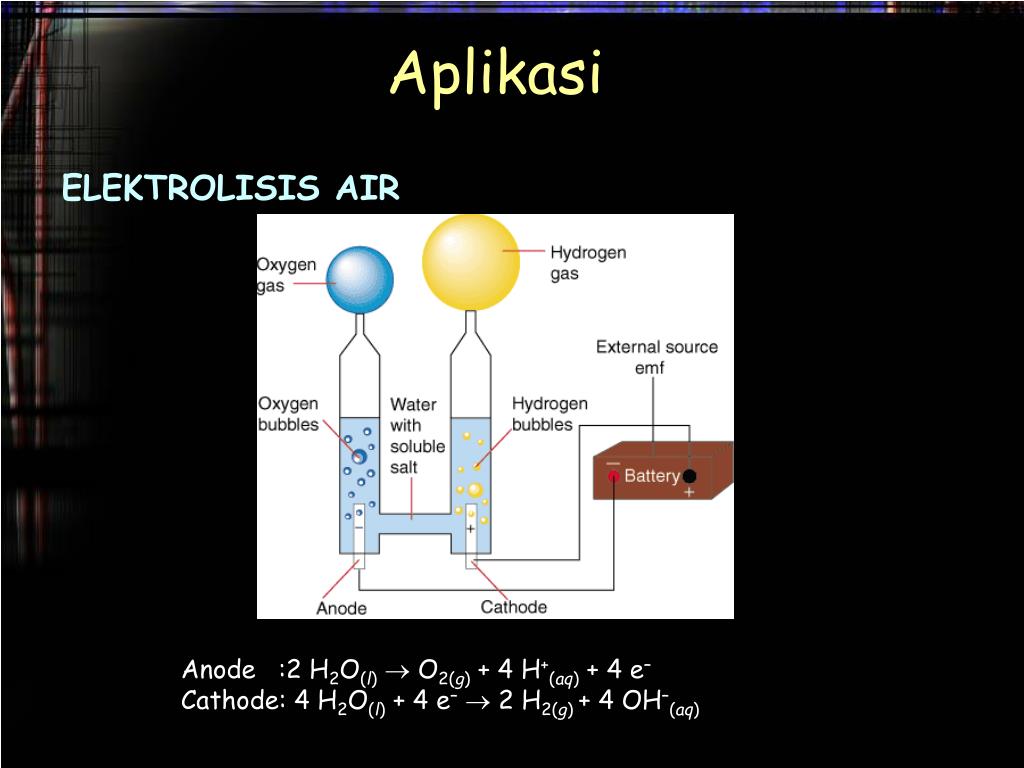
Semoga contoh soal unsur alkali tanah pilihan ganda beserta jawaban dan pembahasannya ini memberikan manfaat yang banyak. Pertanyaan tersebut dapat dijawab berdasarkan nilai potensial elektrode standar. Di katode dihasilkan gas hidrogen. Baterai aki yang sedang diisi kembali (recharge) mengubah energi listrik yang diberikan menjadi produk berupa bahan kimia yang diinginkan.air, h 2 o, dapat diuraikan dengan menggunakan listrik dalam sel elektrolisis. Modul, rumus, & soal elektrokimia.
 Source: brainly.co.id
Source: brainly.co.id
Hukum ohm, tegangan peruraian, tegangan polarisasi, tegangan berlebih dan potensial standar. Pernyataan berikut ini yang benar tentang zat yang teroksidasi di anoda dan tereduksi di katoda pada proses elektrolisis larutan dan lelehan adalah. Dibuat dari elektrolisis larutan garam kloridanya. F = jumlah arus listrik dalam satuan faraday. Logam alkali yang terbentuk berupa zat padat dianoda.
 Source: brainly.co.id
Source: brainly.co.id
Apakah kamu sedang mencari pembahasan mengenai materi elektrolisis? Jadi pernyataan yang benar adalah. Mereka adalah berilium (be), magnesium (mg), kalsium (ca), stronsium (sr), barium (ba), dan radium (ra). Pertanyaan tersebut dapat dijawab berdasarkan nilai potensial elektrode standar. Di anode dihasilkan gas oksigen.
 Source: websiteedukasi.id
Source: websiteedukasi.id
Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal. Di katode dihasilkan gas hidrogen. Soal ini diselesaikan dengan hukum faraday i, dengan rumusan: Reduksi ion alkali terjadi di anoda. Dalam elektrolisis larutan cuso 4, diharapakan logam cu dapat mengendap sebanyak 2,54 g pada katode.
 Source: brainly.co.id
Source: brainly.co.id
Elektrokimia merupakan salah satu materi kimia yang cukup menarik untuk dibahas. F = jumlah arus listrik dalam satuan faraday. Reduksi ion logam alkali terjadi dianode. Ion logam alkali mengalami reaksi reduksi. Bagaimana senyawa kovalen polar dapat menghantarkan listrik?
 Source: brainly.co.id
Source: brainly.co.id
Memahami,menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural berdasarkan rasa ingintahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasankemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang. Di anode dihasilkan gas oksigen. Digunakan katode karbon dan anode dari besi. Pada elektrolisis cuso 4 dihasilkan 25,4 gram endapan cu pada katoda. Pada elektrolisis anode dihubungkan dengan kutub positif sumber energi listrik, sedangkan katode dihubungkan dengan kutub negatif.
 Source: brainly.co.id
Source: brainly.co.id
Ion logam alkali yang terbentuk berupa zat padat di anode. Di katode dihasilkan gas hidrogen. Ion logam alkali mengalami reaksi reduksi. Memahami,menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural berdasarkan rasa ingintahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasankemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang. Jadi pernyataan yang benar adalah.
 Source: studyassistant-id.com
Source: studyassistant-id.com
Dibuat dari elektrolisis larutan garam kloridanya. Sekian dulu pembahasan mengenai elektrolisis, tinggalkan komentar jika ada yang dirasa kurang jelas, semoga bermanfaat. Semoga contoh soal unsur alkali tanah pilihan ganda beserta jawaban dan pembahasannya ini memberikan manfaat yang banyak. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal. Tak lupa, telah tersedia pula latihan soal yang bisa coba kamu kerjakan.
 Source: brainly.co.id
Source: brainly.co.id
Memahami,menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural berdasarkan rasa ingintahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasankemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang. Di katode dihasilkan gas hidrogen. Pernyataan yang tepat tentang pembuatan logam alkali secara elektrolisis adalah. Berapa volume gas h 2 pada 0 0 c tekanan 1 atm, yang dibebaskan pada elektrolisis larutan h 2 so 4 encer dengan jumlah arus yang sama ( ar s = 32 cu 63,5 o = 16) Modul, rumus, & soal elektrokimia.
 Source: id.gprectifier-ar.com
Source: id.gprectifier-ar.com
Digunakan katode karbon dan anode dari besi. Kami juga telah menyediakan soal latihan yang bisa dikerjakan untuk mengasah kemampuanmu. Arus listrik digunakan untuk melangsungkan reaksi redoks tak spontan. Supaya lebih paham mengenai sel elektrolisis, perhatikan 10 contoh soal elektrolisis kelas 12 berikut ini: Memahami,menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural berdasarkan rasa ingintahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasankemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang.
 Source: slideserve.com
Source: slideserve.com
Digunakan katode karbon dan anode dari besi. Pada elektrolisis cuso 4 dihasilkan 25,4 gram endapan cu pada katoda. Supaya lebih paham mengenai sel elektrolisis, perhatikan 10 contoh soal elektrolisis kelas 12 berikut ini: Pertanyaan ini menjadi sumber inspirasi untuk mengembangkan konsep penting dan berguna tentang potensial. Logam alkali yang terbentuk berupa zat padat di anoda.
This site is an open community for users to do submittion their favorite wallpapers on the internet, all images or pictures in this website are for personal wallpaper use only, it is stricly prohibited to use this wallpaper for commercial purposes, if you are the author and find this image is shared without your permission, please kindly raise a DMCA report to Us.
If you find this site helpful, please support us by sharing this posts to your own social media accounts like Facebook, Instagram and so on or you can also save this blog page with the title pertanyaan tentang elektrolisis by using Ctrl + D for devices a laptop with a Windows operating system or Command + D for laptops with an Apple operating system. If you use a smartphone, you can also use the drawer menu of the browser you are using. Whether it’s a Windows, Mac, iOS or Android operating system, you will still be able to bookmark this website.





